Батаева Д.С., Зайко Е.В.
«ФЕДЕРАЛЬНЫЙ НАУЧНЫЙ ЦЕНТР ПИЩЕВЫХ СИСТЕМ ИМ. В.М.ГОРБАТОВА» РАН
Ключевые слова: риски, мясо и продукты убоя животных, антибактериальные препараты, устойчивость микроорганизмов к антибактериальным препаратам.
Аннотация
Определены риски, связанные с наличием в мясе и в продуктах убоя животных остаточных количеств антимикробных препаратов. Один из них — это возникновение устойчивости к антимикробным препаратам патогенных и условно-патогенных микроорганизмов, выделенных из мяса и продуктов убоя животных. Было установлено, что E.coli, микроорганизмы рода Salmonella и Pseudomonas устойчивы к ампициллину, тетрациклину, тилозину и цефалолексину. Однако L.monocytogenes не обладали устойчивостью к этим препаратам. Также установлено, что при попадании в организм животного антимикробные вещества больше всего накапливаются в печени и в почках животного, затем в мясе и меньше всего в жире. Определено, что до 65 % исследованных образцов в той или в иной степени контаминированы антимикробными препаратами.
Введение
Стратегической целью продовольственной безопасности России является обеспечение ее населения безопасной пищевой продукцией. С увеличением потребности населения в мясе и в мясных продуктах необходимо увеличивать их производство. Это возможно при определенном уровне поголовья животных и интенсификации прироста у них мышечной массы.
Прирост мышечной массы, может быть, достигнут и за счет использования стимуляторов роста, в том числе и антибактериальных препаратов (террамицин, биомицин, бацитрацин и гризин — в качестве кормовых добавок).
Антимикробные препараты (противомикробные препараты, antimicrobial agents) — это химические соединения, которые убивают микроорганизмы или угнетают их рост, но при этом они могут продуцироваться в естественных условиях как грибами (например, пенициллин), так и бактериями (например, тетрациклин) — или могут быть синтетическими или полусинтетическими веществами (например, фторхинолоны и амоксициллин, соответственно). Согласно оригинальному определению лауреата Нобелевской премии Сэлмана Ваксмана (Selman Waksman), термин антибиотики (antibiotics) относится только к естественным продуктам микробного происхождения. Тем не менее, этот термин нередко используется как синоним термина антимикробные средства, независимо от естественного или синтетического происхождения.
Существуют определенные требования к стимуляторам роста животных: они должны иметь короткий период выведения из организма; до убоя должно произойти полное выведение их из тканей и органов животного; отсутствие токсического воздействия на организм; отсутствие отрицательного влияния на нормальную кишечную микрофлору и если в качестве стимуляторов роста используются антимикробные препараты, то они не должны вызывать устойчивости микроорганизмов к ним.
По мере увеличения сроков и масштабов практического применения антимикробных и других химио- терапевтических препаратов также нарастает и число устойчивых к ним штаммов микроорганизмов.
Частота инфекций, вызванных антибиотикорезистентными бактериями, увеличивается среди населения и в медицинских учреждениях, вследствие чего эти инфекции становятся важной медико-санитарной проблемой, которая бросает вызов системам здравоохранения многих стран. В результате чрезмерного и неправильного применения антибиотиков у бактерий, находящихся в организме людей и животных, может развиться устойчивость к этим препаратам, вследствие чего инфекционные заболевания, которые в обычных условиях хорошо поддаются лечению антибиотиками, становится трудно, а иногда и невозможно вылечить. Неудачи лечения приводят к росту заболеваемости и смертности от инфекций, а также к необходимости разрабатывать новые антибиотики, что, в конечном счете, ложится дополнительным бременем на общество. Ежегодно в странах Европейского союза свыше 25 000 человек умирают от инфекций, вызванных антибиотикорезистентными бактериями [1].
Поскольку эта устойчивость не имеет экологических, отраслевых или географических границ, ее появление в одной отрасли или в одной стране приводит к формированию резистентности в других отраслях и в других странах. Предупреждение и сдерживание устойчивости к антибиотикам требует принимать во внимание все факторы риска формирования и распространения такой устойчивости в контексте всех условий, отраслей, учреждений от медицины до использования в производстве пищевых продуктов животного происхождения.
ВОЗ уже давно считает, что применение антибиотиков у сельскохозяйственных животных, масштабы которого во многих странах превышают масштабы использования антибиотиков для лечения больных людей, вносит существенный вклад в формирование проблемы устойчивости к антибиотикам в здравоохранении. Эта ситуация требует информирование общества и выработке специальной политики для сдерживания резистентности к антибиотикам с позиций безопасности пищевых продуктов обращая особое внимание на распространение резистентности через пищевую цепь, которое играет важную, хотя нередко и скрытую роль. Резистентность связанных с пищевыми инфекциями зоонозных бактерий родов Salmonella и Campylobacter несомненно связана с применением антибиотиков у сельскохозяйственных животных; пищевые инфекции, вызванные такими резистентными бактериями, многократно документированы у людей. Возбудители кампилобактериоза очень легко приобретают устойчивость к антибиотикам. Во многих странах кампилобактерии, выделенные из мяса птиц, были резистентны к антибактериальным препаратам, включая фторхинолоны [2].
Заболевания у людей, вызванные штаммами кампилобактерий, устойчивыми к антибиотикам, представляют усугубляющуюся проблему здравоохранения.
Эпидемиология устойчивости к антибиотикам осложняется способностью генов, детерминирующих такую устойчивость, распространяться между различными типами бактерий. Кроме того, резистентные к антибиотикам бактерии могут преодолевать барьеры между сферами деятельности, учреждениями и территориями. Такое распространение может быть связано с людьми, животными, пищевыми продуктами животного происхождения и контаминированными объектами внешней среды.
Особую тревогу вызывает устойчивость к так называемым «критически важным антибиотикам», используемым в медицине.
Поскольку было показано, что применение антибиотиков в качестве стимуляторов роста связано с угрозой для здоровья людей, с 2006 г. в странах Европейского союза прекращено использование всех антибиотиков в качестве стимуляторов роста. Прекращение использования антибиотиков для стимуляции роста животных снижает опасность для здоровья людей без какого-либо вреда для здоровья животных или экономических потерь в производстве продуктов животного происхождения.
Очень важной частью работы по сдерживанию резистентности является нормативная регламентация применения антибиотиков у сельскохозяйственных животных. Предлагается, чтобы ветеринарные, сельскохозяйственные и фармацевтические органы рассмотрели возможность принятия следующих мер: прекращение использования антибиотиков в качестве стимуляторов роста животных; применение антибиотиков у животных только по назначению ветеринара; применение антибиотиков, имеющих чрезвычайное значение в медицине (особенно фторхинолонов и цефалоспоринов третьего и четвертого поколений) у сельскохозяйственных животных только при наличии для этого веских оснований.
Кроме того, антибиотики и продукты их метаболизма могут стать причиной аллергии и симптомов отравления, угнетать активность полезной микроф- лоры, способствовать развитию грибковых заболеваний. У человека, регулярно питающегося продуктами, содержащими антибиотики, перегружаются печень и почки, в связи, с чем возрастает риск развития хронических заболеваний, лечение которых осложняется все той же устойчивостью микроорганизмов к антибиотикам.
Использование при производстве сырокопченой продукции, мяса даже с остаточными количествами антибактериальных препаратов влечет за собой невозможность производства качественной и безопасной продукции, т.к. процессы естественной и направленной ферментации и созревания будут ими ингибированы [3].
Целью данной работы являлось определение рисков, связанных с наличием в мясе и в продуктах убоя животных остаточных количеств антимикробных препаратов и выявление антибиотикоустойчивых штаммов.
В соответствии поставленной цели были определены следующие задачи:
- Провести исследование мяса и продуктов убоя животных на наличие остаточных количеств антимикробных препаратов.
- Установить чувствительность микроорганизмов, выделенных их мяса и продуктов убоя, к антимикробным препаратам.
Материалы и методы
В качестве объектов при исследовании наличия остаточных количеств антимикробных препаратов были использованы мясо (область шейного зареза) и продукты убоя (печень, почки и внутренний жир) крупного рогатого скота (КРС) из 5 хозяйств Центральной части России. В качестве тест-агара для определения остаточных количеств антимикробных препаратов использовали плотную культуральную среду по Кундрату со спорами Bacillus stearothermophilus. Устойчивость к антибиотикам (ампициллин, тетрациклин, тилозин, цефалолексин) определяли следующих микроорганизмов: E.coli, L.monocytogenes, Salmonella, Pseudomonas spp..
Отбор образцов мяса и продуктов убоя животных проводили в цехе убоя деструктивным методом. Каждый отобранный образец упаковывали в индивидуальную упаковку, охлаждали и затем доставляли в лабораторию на исследование. Образцы отбирали от 5 животных из каждого хозяйства.
Пробоподготовку проводили, отбирая с поверхности и глубины (суммарно) лабораторной пробы с помощью стерильных ножниц и пинцетов анализируемую пробу массой 50,0–100,0 г и измельчая ее на ротационном гомогенизаторе.
В пакет для гомогенизации вносили (25,0 ± 0,5) г измельченной анализируемой пробы добавляли 25 см3 физиологический раствор и тщательно перемешивали, получая при этом исходную суспензию. Затем емкость с исходной суспензией выдерживали в термостате при температуре (37 ± 1) °C в течение 90 мин, периодически тщательно перемешивая.
Часть исходной суспензии после термостатирования переносили в центрифужные пробирки и центрифугировали при 3000 об/мин в течение 10 мин. Полученную надосадочную жидкость отбирали в стерильные пробирки.
Наличие остаточных количеств антимикробных препаратов определяли следующим образом: надосадочную жидкость вносили параллельно в две лунки культуральной среды по Кундрату с помощью автоматической пипетки по 0,05 см3.
Чашки Петри с исследуемым материалом выдерживали при комнатной температуре не менее 30 мин для диффузии надосадочной жидкости в агар, затем инкубировали в термостате при температуре (65 ± 1) °C в течение (3,5 ± 0,5) ч крышками вверх.
Отсутствие роста тест-культуры, подтверждаемое сохранением синего цвета среды в зоне шириной 2,0 мм и более, оценивали как положительный результат, т. е. как наличие антибиотиков или других антимикробных химиотерапевтических веществ в анализируемой пробе.
Отсутствие роста тест-культуры, подтверждаемое сохранением синего цвета среды в зоне шириной менее 2,0 мм, или наличие роста тест-культуры с изменением цвета среды с синего на желтый, оценивали как отрицательный результат, т.е. как отсутствие антибиотиков или других антимикробных химиотерапевтических веществ в анализируемой пробе.
Устойчивость микроорганизмов к антимикробным препаратам изучали с помощью макрометода серийных разведений в бульоне. Для определения наличия роста микроорганизма пробирки с посевами просматривают в проходящем свете. Рост культуры в присутствии антимикробных препаратов сравнивали с референтной пробиркой («отрицательный» контроль), содержащей исходный инокулюм.
Результаты и обсуждение
При исследовании мяса и продуктов убоя от КРС из пяти хозяйств на наличие остаточных количеств антимикробных препаратов были получены результаты, представленные на рисунке 1.
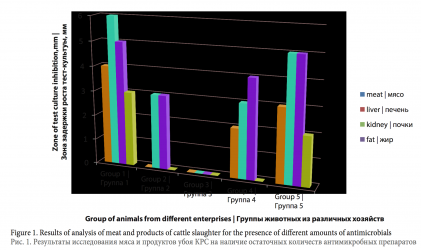
Прежде всего, данные представленные на рисунке 1 показывают, что существует проблема в использовании антимикробных препаратов в нашей стране, т.к. только в одном хозяйстве из пяти исследованных, полностью отсутствовали эти препараты в мясе и в продуктах убоя животных (No 3). Однако и в мясе и в продуктах убоя, полученных от животных из хозяйства No 1 и 5, они были выявлены.
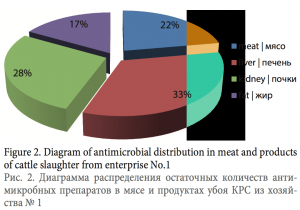
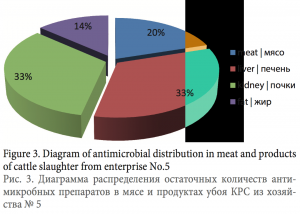
Анализируя эти данные (рис. 2 и 3), было установлено, что распределение антимикробных препаратов в мясе и продуктах убоя от одного животного следующее: в печени — 33 %, в почках — 28–33 %, в мясе — 20–22 %, и меньше всего в жире — 14–17 %.
Например, в работе Закревского В.В. и Лелеко С.Н., которые проводили оценку мясного сырья, поступающего на мясоперерабатывающие предприятия Санкт- Петербурга из разных стран мира, приведены данные исследования говядины, произведенной в РФ, на наличие остаточных количеств антибиотиков (тетрациклин, стрептомицин и левомицетин). Авторами было установлено, что 25 % исследованных образцов говядины были контаминированы [4].
В наших исследованиях бы использован скрининговый метод, с помощью которого можно обнаружитьне только эти антибиотики. Поэтому, мы предполага- ем, что процент контаминированных образцов по ре- зультатам наших исследований был больше.
На основании вышеизложенного можно сказать что, мясо и продукты убоя КРС контаминированы антимикробными препаратами, и чтобы исключить переработку и реализацию такого сырья, необходимо проводить оценку на наличие остаточных количеств антибиотиков и других антимикробных химиотера- певтических веществ [5].
ВОЗ подготовила список антибиотиков «критиче- ски важных» для медицины. К таким приоритетным антибиотикам, в отношении которых нужно срочно осуществлять стратегии снижения риска, относятся фторхинолоны, цефалоспорины третьего и четвертого поколений и макролиды [1]. Это означает, что если к этим препаратам разовьется устойчивость у микроорганизмов.
При определении рисков, связанных с наличием остаточных количеств антимикробных препаратов была изучена устойчивость к антибиотикам микроорганизмов выделенных из мяса и в продуктах убоя животных. Результаты представлены в таблице 1.
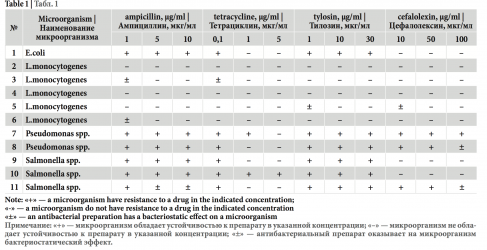
На основании проведенных исследований установлено, что грамотрицательная микрофлора, выявленная из мяса и продуктов убоя животных, обладает устойчивостью к антимикробным препаратам: E. coli, Salmonella и Pseudomonas к ампициллину в дозировке 1–10 мкг/см3, к тилозину в дозировке 1–30 мкг/см3, а Pseudomonas устойчив еще и к цефалолексину в дозировке 10–100 мкг/см3, к тетрациклину в дозировке 0,1– 1,0 мкг/см3. Один из исследованных штаммов Salmonella устойчив еще и к тетрациклину в дозировке 0,1–5,0 мкг/ см3, а другой только в дозировке 0,1 мкг/см3. Штаммы L.monocytogenes не обладали устойчивостью к антибиотикам.
Например, штаммы E. coli животного и водного происхождения, контаминирующие пищевые продукты, могут быть носителями генов резистентности, которые могут быть переданы бактериям, обитающим в организме людей, или другим патогенным микроорганизмам во время их пребывания в кишечнике. Если устойчивый штамм E. coli колонизирует организм человека и вызывает развитие заболевания или передает гены резистентности патогенным бактериям, обычное лечение будет неэффективным, что приведет более длительному и тяжелому течению заболеванию.
Косвенные угрозы возникают, когда гены резистентности передаются в организме животных от устойчивых бактерий — таких как E. coli или представители рода Enterococcus — к бактериям, патогенных для людей. Гены резистентности могут легко передаваться от одних бактерий к другим, обитающих у наземных животных, рыб и людей. Более того, такой перенос может происходить в различных условиях окружающей среды, например на кухнях, в помещениях для содержания животных или в водоемах [6].
Пищевые продукты, преимущественно животного происхождения, являются важным резервуаром антибиотикорезистентных сальмонелл, которые могут передаваться от сельскохозяйственных животных к человеку. Более того, среди некоторых сероваров сальмонелл широко распространена полирезистентность (устойчивость к антибиотикам более чем четырех классов), особенно среди штаммов S. typhimurium — как в глобальных масштабах, так и в Европейском регионе [7].
Выводы
Установлено что:
- На переработку поступает мясо и продукты убоя животных контаминированных антимикробными препаратами;
- Микроорганизмы, выделенные из мяса и продуктов убоя животных, обладают устойчивостью к антимикробным препаратам.
- Распределение антимикробных препаратов в мясе и продуктах убоя животного следующее: в печени — 33 %, в почках — 28–33 %, в мясе — 20–22 %, в жире — 14–17 %.
Почти 80 % животноводческих хозяйств не выдерживают сроки перед направлением на убой КРС после использования антимикробных препаратов Таким образом, есть определенный риск при наличии антибиотиков и других антимикробных химиотерапевтических веществ в мясе и в продуктах убоя животных, как для здоровья человечества, так и для переработчиков мяса. Риск заключается в том что, бесконтрольное использование антимикробных препаратов в ветеринарии и в животноводстве приведет к увеличению устойчивых к антибиотикам штаммов микроорганизмов, а у переработчиков мяса возникнут проблемы с выпуском качественной и безопасной продукции.
Полученные результаты исследований позволяют рекомендовать на ветеринарной точке осмотра внутренних органов проводить отбор проб печени, почек, жира и мяса для качественной оценки наличия остаточных количеств антибиотиков и других антимикробных химиотерапевтических веществ.
Такой анализ можно провести, используя экспресс-метод, представленный и использованный при выполнении данной работы. Он позволяет, не имея дорогостоящего оборудования, в условиях производственной лаборатории провести испытание мяса и продуктов убоя животных и в течение 5–6 часов определить остаточные количества антибиотиков и других антимикробных химиотерапевтических веществ без видовой и количественной идентификации и принять быстрое решение о дальнейшем использовании мясного сырья.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- European Centre for Disease Prevention and Control. The bacterial challenge: time to react — a call to narrow the gap between multidrug-resistant bacteria in the EU and the development of new antibacterial agents. Stockholm, 2009. — 54P. www. ecdc.europa.eu www.emea.europa.eu.
- European Food Safety Authority. The Community summary report on antimicrobial resistance in zoonotic agents from animals and food in the European Union in 2004–2007. EFSA Journal, 2010, 8(4):1309–1615.
- Басова Е. Война миров: антибиотики в сельском хозяйстве. Информационное агентство DairyNews (ООО «Новости молочного рынка»), 2012. 4. Закревский, В.В. Современная лабораторная диагностика антибиотиков и нтрофуранов в мясных продуктах / В.В. Закревский, С.Н. Лелеко // Материалы девятой Международной научной конференции «Донозология — 2013. Факторы риска и здоровье населения при использовании наноматериалов и нанотехнологий» / под общ. ред. д.м.н., проф. М.П. Захарченко. — СПб.: Крисмас+, 2013.— С. 136–138.
- Минаев М.Ю., Батаева Д.С., Еремцова А.А. Технологические риски, связанные с образованием стафилококкового энтеротоксина при производстве сухих сырокопченых колбасах, выработанных с применением стартовых культур// Мясная индустрия. 2015. No 12. с.24–28.
- Kruse H, Sørum H. Transfer of multiple drug resistance plasmids between bacteria of diverse origins in natural microenviron- ments. Applied and Environmental Microbiology, 1994, 60(11): 4015–4021.
- European Centre for Disease Prevention and Control et al. Joint opinion on antimicrobial resistance (AMR) focused on zoonotic infections. Scienti c Opinion of the European Centre for Disease Prevention and Control; Scienti c Opinion of the Panel on Biological Hazards; Opinion of the Committee for Medicinal Products for Veterinary Use; Scienti c Opinion of the Scienti c Committee on Emerging and Newly Identi ed Health Risks. EFSA Journal, 2009, 7(11):1372 (http://www.efsa.europa. eu/it/efsajournal/doc/1372.pdf, accessed 21 January 2011).